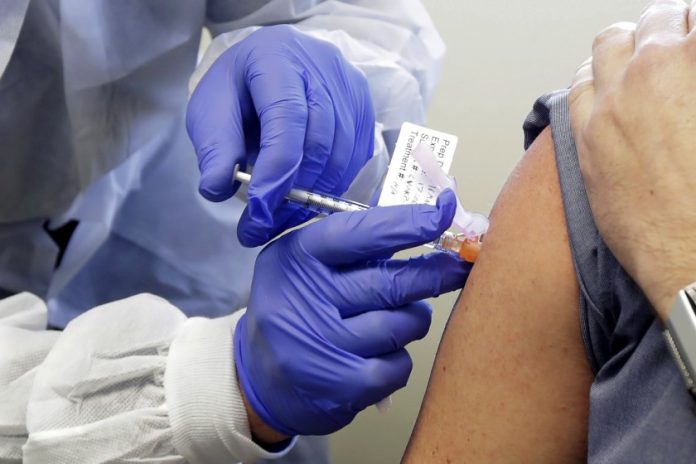
路透7月13日 – 辉瑞(PFE.N)和其伙伴BioNTech SE (22UAy.F) (BNTX.O)周一表示,他们的两种实验性新冠病毒候选疫苗获得美国食品药物管理局(FDA)指定“快速通道”,获得该身分可加速监管审核程序。
此消息拉抬普遍市场人气,投资人为新冠肺炎疫苗研发有进展的迹象感到振奋。BioNTech在美上市股票一度大涨约15%,最后收升10.55%。辉瑞股价一度涨约5%,终场收高4.08%报35.21美元。
FDA授予快速通道,将加快显示有潜力因应尚未满足的医疗需求的新药及疫苗的审核。
摩根大通分析师Cory Kasimov在一篇报告指出,市场“迫切希望抓住疫苗领域的任何正面进展”。
但Kasimov表示,最新消息实际上并没有那么令人惊讶或那么意义重大,并指出获得FDA指定快速通道“不意味着有可能成为一种特定的候选疫苗。”
在美国和德国目前进行的试验中,公司所评估的至少四种疫苗中,获得指定的这两种候选疫苗BNT162b1和BNT162b2是最先进的。
这两家公司称,他们预计最早本月稍晚会开始对至多3万名参与者进行大规模试验,这还要取决于监管批准。
如果疫苗成功,他们将加倍努力,争取到今年年底生产出高达1亿剂,到2021年底有可能生产超过12亿剂。