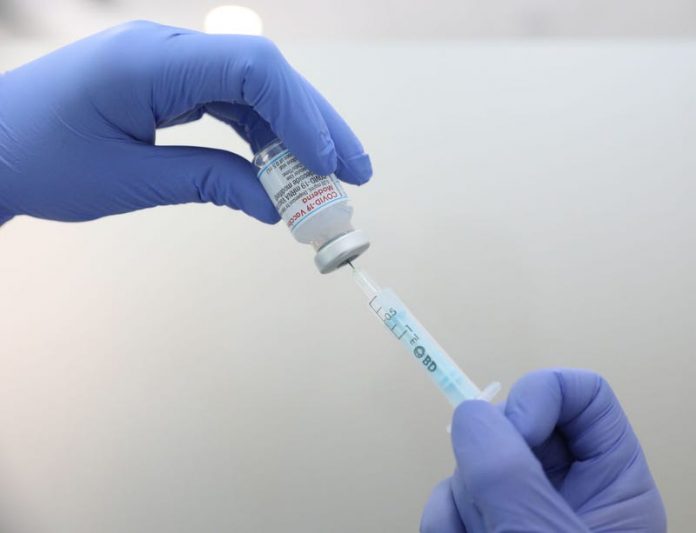
【美洲华联社8月31日洛杉矶报道】美国食品和药物管理局(FDA)周三授权辉瑞和Moderna 开发的 COVID-19疫苗的更新版本,以针对 Omicron 病毒株。
据KNX报道,尽管缺乏人体试验的数据,但这些注射应该在劳工之后提供。 FDA批准了重组后的 mRNA 疫苗,因为辉瑞公司表示其人体试验正在进行中。
BA.5 变体包括目前在美国报告的大多数 COVID 病例,新疫苗直接针对该菌株。
不过这一批准没有得到 FDA 咨询委员会的意见,这表明该机构的新方法将反映流感疫苗。两家公司上周都提交了紧急授权请求。
更新后的配方包括每家公司的原始疫苗和针对 BA.4 和 BA.5 变体的新疫苗。辉瑞的疫苗是30微克,可以给12岁或以上的人接种。 Moderna的50微克剂量被授权用于 18 岁及以上的成年人。
疾病控制和预防中心仍必须建议批准疫苗,以便他们投入使用。疾病预防控制中心的疫苗咨询小组周四开会进行预期投票。
一些医护人员担心,如果没有更多信息,公众会犹豫是否接受重新格式化的疫苗。
F